Der Grammatik biologischer Zellen auf der Spur
Zellen im Körper tauschen eine Vielzahl von Signalen mit ihrer Umgebung aus. Defekte Signalwege können die Funktion von Zellen beeinträchtigen und Krankheiten auslösen. Heutzutage kennt man jedoch kaum mehr als die Vokabeln der zellulären Sprache, nicht aber wie „Worte“ in „Sätzen“ zusammenwirken. Wäre die Zell-Grammatik bekannt, könnte man die komplexen Abläufe in Zellen erst wirklich verstehen. Forscher des KIT haben im Fachmagazin Angewandte Chemie eine Methode vorgestellt, um die Grammatik der Zellsignale zu entschlüsseln.
MOSAIC-Methode: ganze Sätze der Zellsprache entschlüsseln
„Rezeptoren auf Zellmembranen reagieren auf eine Vielzahl von Signalmolekülen. Diese bilden das Vokabular der Kommunikation“, erklärt Christof Niemeyer vom Institut für Biologische Grenzflächen des KIT. In der Regel werden mehrere, räumlich verteilte Rezeptoren gleichzeitig angesprochen. „Mit unserer neuen MOSAIC-Methode können wir nun gezielt nicht nur Vokabeln, sondern ganze Sätze der Zellsprache entschlüsseln.“
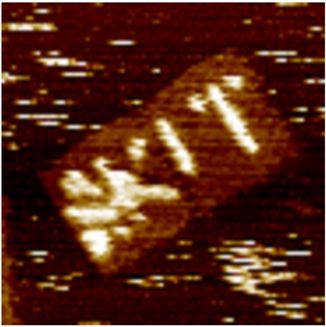
Um eine einzelne Zelle mit einem definierten Satz anzusprechen, haben Niemeyer und sein Team zunächst die gewünschten Signalmoleküle mit einer Genauigkeit von 5 Nanometern auf einer Art Stecktafel fixiert, die etwa 100 Nanometer lang ist. Anschließend wurden Dutzende dieser Stecktafeln auf dem Zellträger aufgebracht. Damit ist es nun erstmals möglich, auf einer größeren Fläche viele Moleküle mit Nanometergenauigkeit zu positionieren. „Entscheidend war, dass wir sowohl die Selbstorganisation von Molekülen als auch eine mikroskopische Drucktechnik in der MOSAIC-Methode (Multiscale Origami Structures as Interfaces for Cells) vereinen konnten“, so Niemeyer.
Grundlagen für Therapieansätze und Medikamentenentwicklungen
„Viele Krankheiten wie Krebs oder Autoimmun-Erkrankungen lassen sich auf die Fehlfunktion von Rezeptoren und Signalen in Zellen zurückführen. Komplexe Signalwege zu verstehen, legt also die Grundlagen für kommende Therapieansätze und Medikamentenentwicklungen“, betont Niemeyer.
Literatur: Multiscale Origami Structures as Interface for Cells (pages 15813–15817), Alessandro Angelin, Simone Weigel, Ruben Garrecht, Dr. Rebecca Meyer, Jens Bauer, Ravi Kapoor Kumar, Dr. Michael Hirtz and Prof. Dr. Christof M. Niemeyer, DOI: 10.1002/anie.201509772, onlinelibrary.wiley.com/doi/10.1002/anie.201509772/abstract
Weitere Informationen in der Pressemitteilung 038/2016
kes, 16.03.2016